

如何才能更有效地把一個(gè)大分子(如蛋白質(zhì)或核酸)送入細(xì)胞,?很多年來(lái),這個(gè)問(wèn)題不僅難住了無(wú)數(shù)研究人員,,也讓整個(gè)醫(yī)藥業(yè)備受困擾,。然而,因?yàn)閷?shí)驗(yàn)室的一個(gè)意外發(fā)現(xiàn),,Armon Sharei博士卻找到了一個(gè)看上去異?!昂?jiǎn)單”的解決方案:給細(xì)胞一個(gè)“溫柔”的擠壓。
如今,,Armon Sharei博士創(chuàng)立的SQZ Biotechnologies公司正在利用這種技術(shù)打造新一代細(xì)胞療法,,靶向癌癥等各種疾病。在今天的這篇文章里,,藥明康德內(nèi)容團(tuán)隊(duì)與Sharei博士進(jìn)行了一次深入交流,,請(qǐng)他談一談這種創(chuàng)新療法的前世今生,以及對(duì)于細(xì)胞/基因療法未來(lái)的思考,。
 SQZ Biotechnologies公司創(chuàng)始人兼首席執(zhí)行官Armon Sharei博士
SQZ Biotechnologies公司創(chuàng)始人兼首席執(zhí)行官Armon Sharei博士
得益于生物科技的突飛猛進(jìn),,近些年來(lái),細(xì)胞/基因療法不斷取得新突破,,逐步釋放其醫(yī)療潛力,。其中,腫瘤免疫細(xì)胞治療是一大熱點(diǎn),,而它們目前所使用的基因編輯技術(shù)多依賴于病毒載體(如腺相關(guān)病毒)——病毒的遺傳物質(zhì)能穿透細(xì)胞膜,,進(jìn)入到細(xì)胞內(nèi),,引起感染,因此具有被改造成遞送遺傳物質(zhì)之工具的潛力,。
以嵌合抗原受體T細(xì)胞免疫療法(CAR-T)為例,,該療法是通過(guò)基因工程技術(shù),人工改造腫瘤患者的T淋巴細(xì)胞,,在體外大量培養(yǎng)后生成腫瘤特異性CAR-T細(xì)胞,,再回輸至患者體內(nèi)用以識(shí)別、殺死癌細(xì)胞,。2011年,,一個(gè)名叫Emily Whitehead的小女孩成為全球首個(gè)接受CAR-T細(xì)胞療法的兒童患者:在經(jīng)歷過(guò)急性淋巴性白血病兩次復(fù)發(fā)后,她在命懸一線之際接受了CAR-T療法的治療,,并成功清除了體內(nèi)所有的癌細(xì)胞,。白血病女孩的“重生記”,讓CAR-T療法一時(shí)名聲大噪,。
 明星抗癌療法CAR-T讓Emily Whitehead重獲新生(圖片來(lái)源:Courtesy of the Emily Whitehead Foundation)
明星抗癌療法CAR-T讓Emily Whitehead重獲新生(圖片來(lái)源:Courtesy of the Emily Whitehead Foundation)
對(duì)于以CAR-T為代表的細(xì)胞/基因療法業(yè)已取得的成績(jī),,Sharei博士表示值得肯定,“在某些本已沒(méi)有多少生存機(jī)會(huì)的患者身上,,CAR-T的緩解率或可達(dá)到70%以上,,這令人印象深刻,與化療或靶向療法往往只能讓患者多撐上一兩個(gè)月相比,,它們截然不同,。”
正所謂“甘瓜苦蒂,,天下物無(wú)全美”,。盡管基于病毒載體的細(xì)胞/基因療法亮點(diǎn)不少,但這些載體同樣面臨著成本過(guò)高,、周期過(guò)長(zhǎng)的瓶頸,,它們能夠攜帶的“貨物”種類以及可轉(zhuǎn)導(dǎo)的細(xì)胞類型都非常有限。同時(shí),,單靠病毒載體也無(wú)法將基因精準(zhǔn)地插入到所需的位置,,從而帶來(lái)潛在風(fēng)險(xiǎn)——它們可能會(huì)影響到健康基因的表達(dá),或是導(dǎo)致插入基因被異常調(diào)節(jié),,出現(xiàn)失控。從實(shí)際應(yīng)用來(lái)看,,這類療法往往被局限于治療罕見的遺傳性疾病,。
如果不用借助病毒載體,卻依然能對(duì)細(xì)胞進(jìn)行有效改造,,無(wú)疑將極大地加速細(xì)胞療法的開發(fā),、給整個(gè)領(lǐng)域帶來(lái)革命性的變化,,SQZ的“擠壓”細(xì)胞法走的正是這條路子。
先把臺(tái)歷翻回到11年前,。2008年,,Sharei博士進(jìn)入麻省理工學(xué)院(MIT)攻讀化學(xué)工程博士學(xué)位。他的研究課題是開發(fā)一種將藥物轉(zhuǎn)入細(xì)胞的方法,。一開始,,他設(shè)計(jì)了一把“迷你槍”,想把藥物“打”進(jìn)細(xì)胞,,但效果不怎么樣,。為了提高命中率,他把“槍管”頂在細(xì)胞上進(jìn)行射擊,,結(jié)果卻出乎意料——藥物確實(shí)順利進(jìn)入了細(xì)胞,,但進(jìn)入的多少卻與這把“槍”的射擊力度無(wú)關(guān)。經(jīng)過(guò)不斷地摸索,,Sharei博士等人找出了問(wèn)題的答案:讓藥物進(jìn)入細(xì)胞的,,并不是“迷你槍”的射擊,而是“槍管”的擠壓,。Sharei博士的發(fā)現(xiàn)立刻引起了創(chuàng)業(yè)大牛Robert Langer教授的注意,,他敏銳地意識(shí)到其背后所隱藏的醫(yī)療潛力。在他的建議下,,2013年,,Sharei博士創(chuàng)立了SQZ,其名字的寓意正是“擠壓”,。

如今,,被SQZ稱為“Cell Squeeze”的平臺(tái)使用的是由硅-玻璃制成的微流控芯片,它們可以擠壓細(xì)胞并在細(xì)胞膜上制造臨時(shí)小孔,。這些孔洞很小,,但可以讓各種材料(如蛋白質(zhì)、核酸和碳納米管)順利進(jìn)入,。目前,,SQZ已開發(fā)出了數(shù)十種芯片來(lái)擠壓不同大小的細(xì)胞。通過(guò)這樣的方式,,SQZ專有技術(shù)平臺(tái)在不依靠病毒載體的情況下,,完成了對(duì)細(xì)胞的基因工程改造。
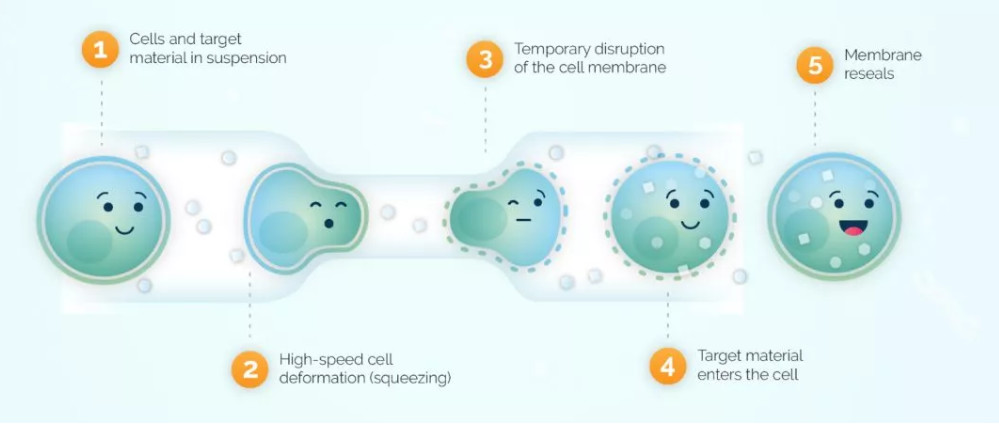 SQZ的細(xì)胞療法技術(shù)平臺(tái)示意圖(圖片來(lái)源:SQZ公司官網(wǎng))
SQZ的細(xì)胞療法技術(shù)平臺(tái)示意圖(圖片來(lái)源:SQZ公司官網(wǎng))
2018年11月,,SQZ在知名學(xué)術(shù)期刊PNAS上發(fā)表了一篇名為“Cell engineering with microfluidic squeezing preserves functionality of primary immune cells in vivo”的科學(xué)論文,,研究結(jié)果表明,使用這種“擠壓”技術(shù)對(duì)細(xì)胞基因表達(dá)的影響很小,,因而能夠保存細(xì)胞的正常功能,,而這些功能對(duì)維持細(xì)胞療法的療效至關(guān)重要,。
2019年10月22日,SQZ又迎來(lái)了一個(gè)好消息,,美國(guó)FDA已批準(zhǔn)該公司開展HPV陽(yáng)性腫瘤臨床試驗(yàn),。其操作流程主要包括:先從患者的血液中提取外周血單核細(xì)胞,然后使用SQZ平臺(tái)賦予其腫瘤抗原,;攜帶HPV陽(yáng)性腫瘤抗原的細(xì)胞被注射回患者體內(nèi),,激活免疫系統(tǒng)的殺傷性T細(xì)胞(CD8陽(yáng)性T細(xì)胞)以攻擊癌細(xì)胞。Sharei博士認(rèn)為,,如果能在HPV陽(yáng)性腫瘤上取得成功,,那么這種療法很有希望被應(yīng)?