

面對干細胞治療的很多不確定性,我們應(yīng)當理性看待,。本文盤點了近14年全球間充質(zhì)干細胞的臨床研究現(xiàn)狀,,包含臨床試驗數(shù)量,細胞來源,,疾病種類,,給藥途徑,專利擁有情況,,細胞劑量等,。
撰文:Cel G
修訂:步步先生
1976年,F(xiàn)reidenstein等人首次發(fā)現(xiàn)在骨髓里存在一群不均一的細胞群,,這種細胞在體外培養(yǎng)時,,呈貼壁生長,形態(tài)和成纖維細胞相似,,呈克隆性增殖,,并提出“骨髓間充質(zhì)干細胞”(Mesenchymalstem cells,MSCs)的概念,。如今,,MSCs已從人類許多其他來源組織中分離和鑒定出來,包括脂肪組織,、骨骼肌,、臍帶血和華爾通膠等。
我們以“干細胞”為關(guān)鍵詞搜索,,在“中國知網(wǎng)數(shù)據(jù)庫”檢索,,得到26萬條結(jié)果。其中,,與“間充質(zhì)干細胞”關(guān)鍵詞相關(guān)的可達32%,,其研究熱度可見一斑。
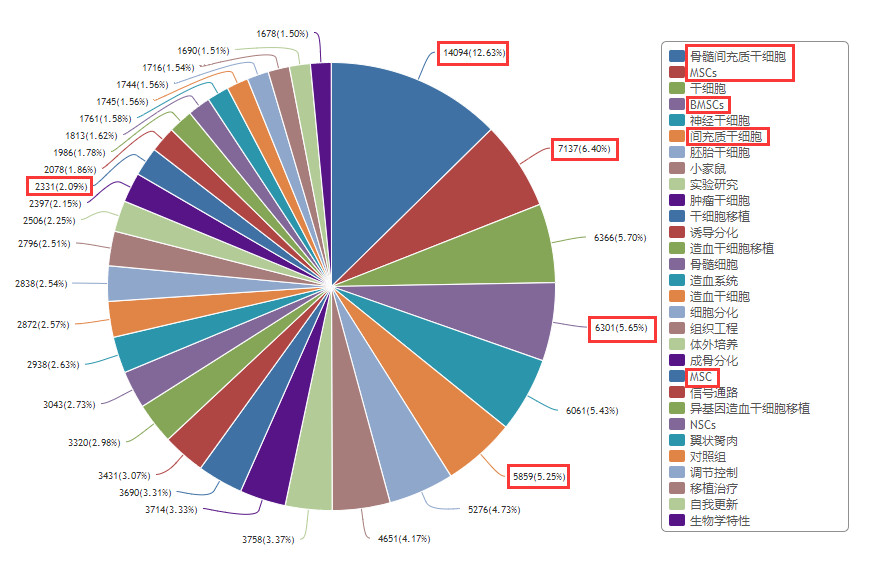 圖1:在知網(wǎng)上搜索“干細胞”,,間充質(zhì)干細胞相關(guān)關(guān)鍵詞占比32%
圖1:在知網(wǎng)上搜索“干細胞”,,間充質(zhì)干細胞相關(guān)關(guān)鍵詞占比32%
近期,,美國學者Maciej Kabat等人在國際期刊《干細胞轉(zhuǎn)化醫(yī)學》上刊登了一篇報道,他們使用關(guān)鍵詞“Mesenchymal”,,對2019年3月19日前登記在美國國立衛(wèi)生研究院(NIH)臨床試驗登記系統(tǒng)(ClinicalTrials.gov)上的914項間充質(zhì)干細胞臨床試驗進行了多維度分析,。
亮點其一就是,針對細胞治療的給藥途徑和使用劑量進行了匯總分析,。這兩種因素以前并未專門提及,,而這是影響細胞治療效果的重要因素,。
經(jīng)統(tǒng)計發(fā)現(xiàn),在2007 - 2012年期間,,全球注冊的MSCs臨床試驗呈快速增長,,隨后進入一個平臺期,在2018年又出現(xiàn)“陡降”,。對此,,本文做一簡單評述。
全球每年新增臨床試驗的數(shù)量,,體現(xiàn)了研究的增量,。而不同階段臨床試驗的占比,也可以看出整體臨床研究的進展:
1期臨床試驗重點考察「安全性」
2期臨床試驗初步考察「有效性」
3期臨床試驗全面考察「有效性」
3期臨床試驗成功后,,新藥就可以申請(上市銷售)了,。其后4期臨床試驗,可以在細胞藥物銷售階段進行,。臨床試驗的“夭折”幾率是非常高的,,特別是進入2/3期的。需要特別指出的是,,出于對患者安全負責的態(tài)度,,安全性評估會貫穿整個1-4期臨床試驗。
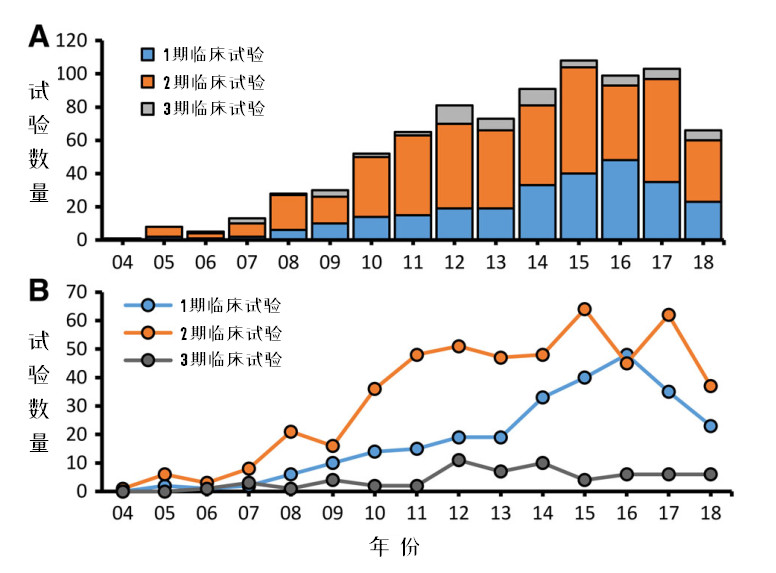 圖2:每年新增臨床試驗,,按階段分類
圖2:每年新增臨床試驗,,按階段分類
圖2是全球MSCs臨床試驗的情況,,A圖反映總量,,B圖反映各個階段臨床試驗的趨勢,。
1期臨床試驗在2014年前呈穩(wěn)步增長趨勢,之后陡升,,到2016年達峰值,,此后有所回落。這一數(shù)據(jù)反映出每年注入整個MSCs 臨床試驗項目的增量,。
縱觀整個臨床試驗,,處于2期的占比最高。從全球MSCs的整體臨床試驗分析,,安全性評估基本都可通過,,但很多臨床試驗都止步于有效性評估。整體趨勢是,,從2007年起開始快速增長,,到2011年以后進入一個相對穩(wěn)定的平臺期。
3期臨床試驗在2012 - 2014年間達到頂峰,,最高達到了近12%的峰值,,此后又回落到6%以內(nèi)的比例,。
目前,完成3期臨床試驗有3種MSCs產(chǎn)品:Mesoblast(已經(jīng)提交上市申請,,尚未獲批),、Alofisel(已在歐盟獲批上市銷售)、Stemirac,。
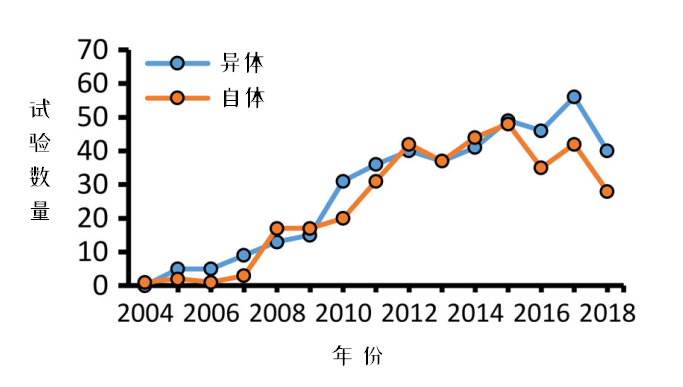 圖3:每年新增臨床試驗,,按自體/異體來源分類
圖3:每年新增臨床試驗,,按自體/異體來源分類
從每年新增的臨床試驗變化看,使用同種異體來源MSCs進行的臨床試驗在2015年,,首次超過了自體,。研究者認為可能與干細胞庫增多有關(guān)。
然而小編不這么認為,,小編發(fā)現(xiàn)可能與MSCs組織來源有關(guān),,因為骨髓和脂肪組織來源的MSCs臨床試驗數(shù)量在減少(圖4),而這兩種組織來源的MSCs是自體應(yīng)用的主力,。從這個角度看,,也解釋了為什么2018年MSCs臨床試驗會“陡降”。
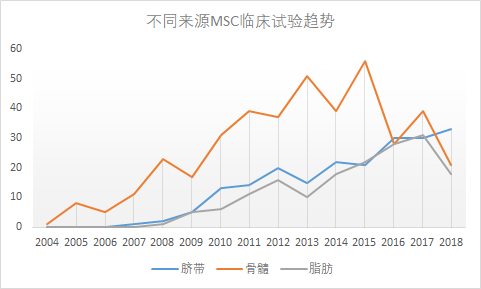 圖4:不同來源MSCs臨床試驗趨勢
圖4:不同來源MSCs臨床試驗趨勢
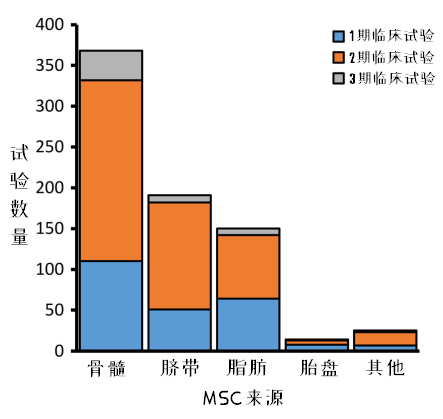 圖5:不同來源的MSCs臨床試驗情況
圖5:不同來源的MSCs臨床試驗情況
在臨床試驗中,,最多使用的MSCs來源于骨髓,,其次分別是臍帶、脂肪和胎盤,。相對而言,,骨髓MSCs研究中,3期臨床試驗的占比最高,。(注:在這里,,研究者將臍帶血來源MSCs統(tǒng)計入了臍帶來源,下文中出現(xiàn)的臍帶也一樣,。)
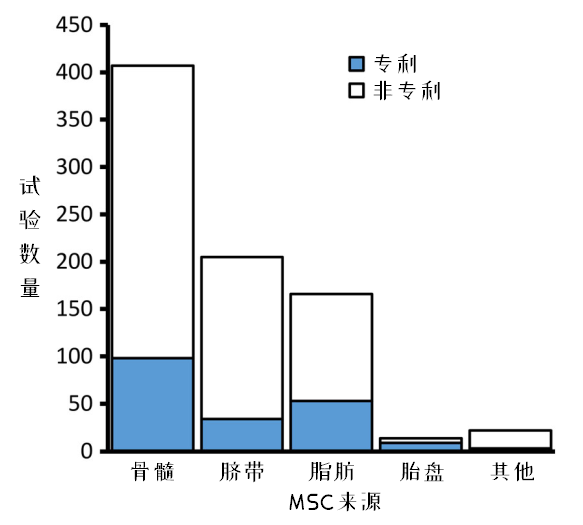 圖6:不同來源MSC臨床試驗的專利化程度
圖6:不同來源MSC臨床試驗的專利化程度
圖6.反映了MSCs臨床試驗中企業(yè)的參與情況,,有24%的臨床試驗擁有專利專利細胞產(chǎn)品。按其比例排序,,胎盤>脂肪>骨髓>臍帶>其他,。
這可能反映了胎盤和脂肪中的MSCs來源更復(fù)雜,制備技術(shù)更多樣化,,相對容易形成專利技術(shù),。
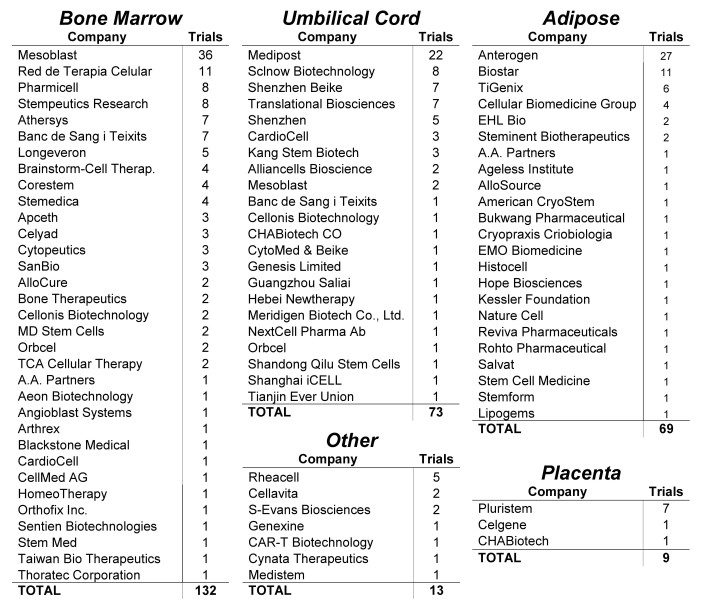 圖7:各公司開展MSC臨床試驗情況
圖7:各公司開展MSC臨床試驗情況
在注冊的MSCs臨床試驗,總共82家公司參與,。有3家開展的臨床試驗就占比30%,,他們分別使用不同組織來源的MSCs產(chǎn)品:Mesoblast(骨髓)、Anterogen(脂肪)和Medipost(臍帶),。
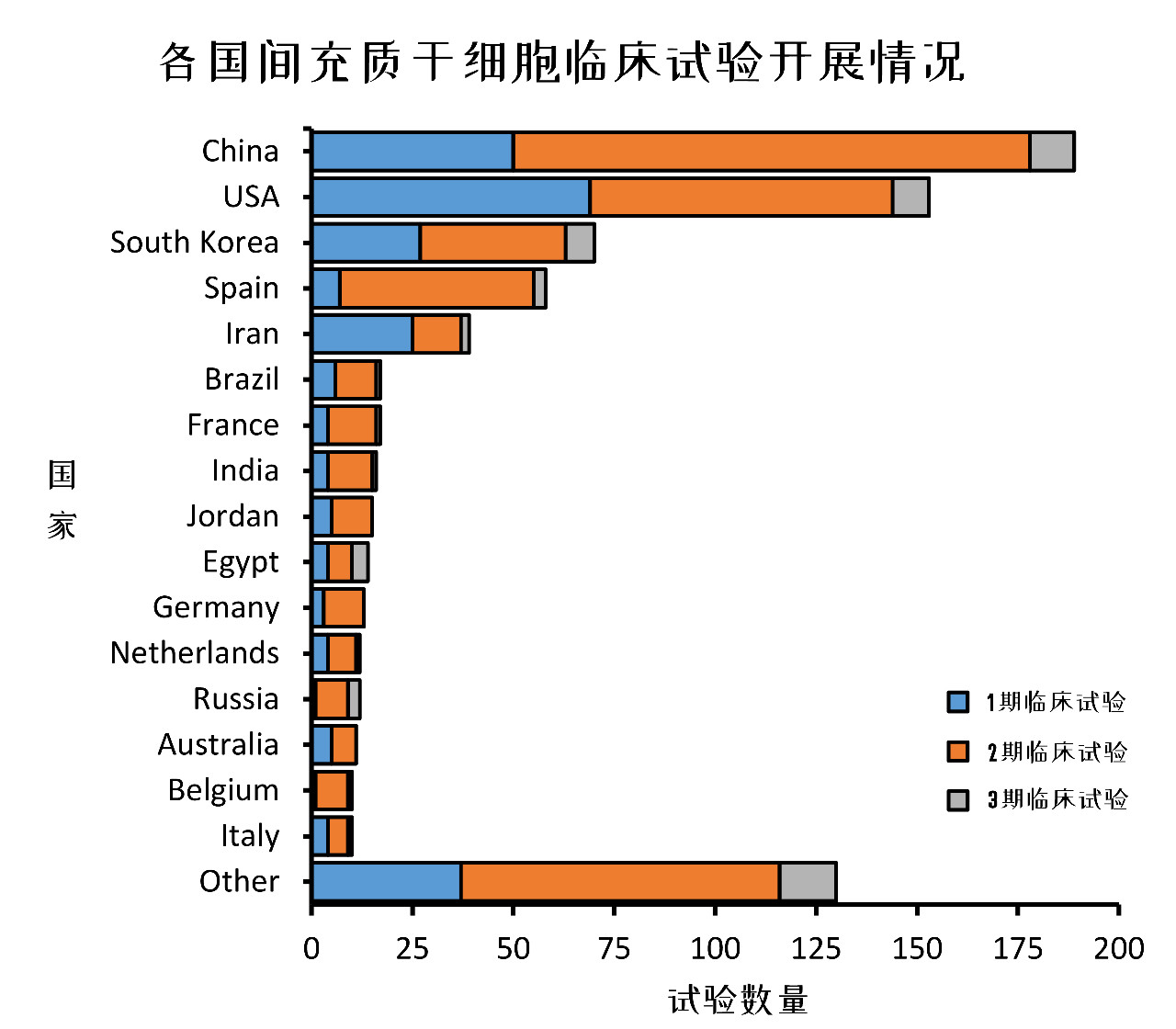 圖8:各國注冊MSCs臨床試驗情況
圖8:各國注冊MSCs臨床試驗情況
從國家來區(qū)分,,中國(22%)的MSCs臨床研究最多,,美國其次(19%)、韓國,、西班牙和伊朗緊隨其后,,歐盟加起來大概占17%。
你沒看錯,,在這張圖上并沒有干細胞研發(fā)強國日本(大概是因為日本以iPSC開發(fā)為主),。
在2005 - 2017年間,日本只開展了6項MSCs臨床試驗,,其中4項使用了脂肪MSCs,,4項治療肝臟疾病,迄今沒有一項進入3期臨床試驗的項目,。
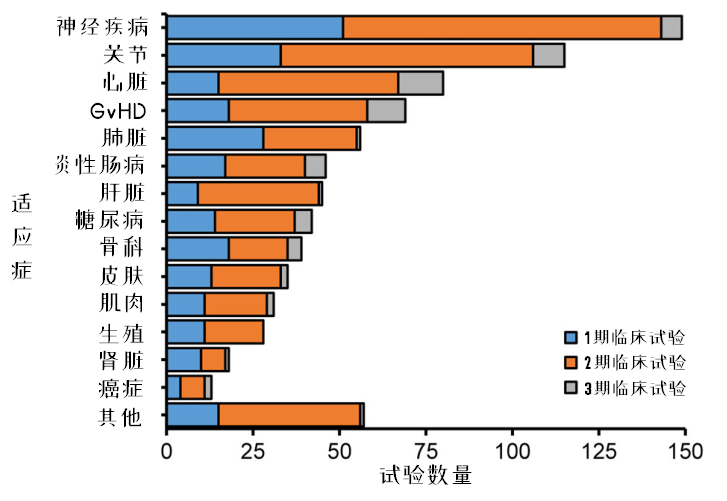 圖9:MSCs臨床試驗適應(yīng)癥的開展情況
圖9:MSCs臨床試驗適應(yīng)癥的開展情況
Maciej Kabat等人將臨床試驗適應(yīng)癥分為14類,,無法分類或數(shù)量太少歸為其他。其中,,在注冊的適應(yīng)癥中,,神經(jīng)系統(tǒng)疾病(17%)和關(guān)節(jié)疾病(15%)最多,其次是心臟疾病(8.8%)和GvHD(8.3%),,后兩者的3期臨床試驗占比更高,。
剩下的適應(yīng)癥大致分為:
占比5%左右:糖尿病、炎性腸病,、骨科,、肝臟、肺部疾??;
占比3%左右:肌肉、生殖,、皮膚疾??;
占比更低:敗血癥,、癌癥、血液,、腎臟疾病,。
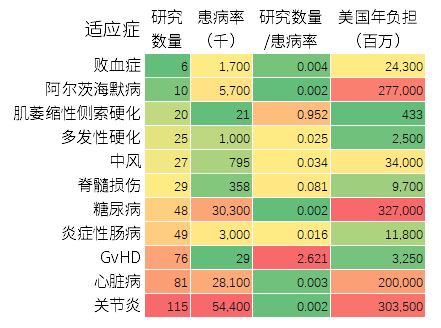 圖10:MSCs臨床試驗的適應(yīng)癥與患病率的關(guān)系
圖10:MSCs臨床試驗的適應(yīng)癥與患病率的關(guān)系
研究者還統(tǒng)計了某些疾病的患病率及其給美國社會帶來的經(jīng)濟負擔,并和相應(yīng)的研究數(shù)量進行了對比,。年負擔能體現(xiàn)相應(yīng)細胞產(chǎn)品的市場前景,,糖尿病、關(guān)節(jié)炎,、阿爾茨海默癥和心臟病排在前列,。
從研究數(shù)量與患病率的對應(yīng)相關(guān)性來看,,GvHD研究最多,肌萎縮側(cè)索硬化癥次之,。對應(yīng)相關(guān)性偏少的適應(yīng)癥有:敗血癥,、阿爾茨海默癥、糖尿病,、心臟病和關(guān)節(jié)炎,。
關(guān)于關(guān)節(jié)炎、心臟病和糖尿病的注冊MSCs臨床試驗的絕對數(shù)量排在第1,、第2.和第5位,,但患病率卻大大高于其他疾病,這是其對應(yīng)相關(guān)性偏少的原因,。而敗血癥則可能是現(xiàn)有治療手段能解決問題,,由于市場份額小,因此研究少,。
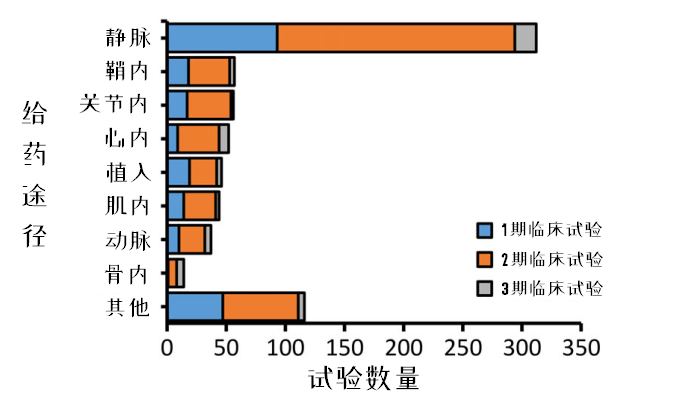 圖11:區(qū)分給藥途徑的MSC臨床試驗開展情況
圖11:區(qū)分給藥途徑的MSC臨床試驗開展情況
在914項臨床試驗中,,只有84%能明確給藥途徑。
在目前已知的8種給藥途徑中,,主要通過循環(huán)系統(tǒng)給藥(其中靜脈占43%,,動脈占5%)。靜脈輸注由于操作簡便,、侵襲性小,、可重復(fù)性強,所以治療中最常使用,。
此外,,有36項試驗(4.6%)進行了兩種以上的給藥途徑。
有多項臨床試驗使用了生物材料或基質(zhì)來遞送MSCs,,在圖中以“植入”代表其給藥方式,。3期臨床試驗占比最高的給藥途徑分別是靜脈給藥、骨內(nèi)給藥(骨髓腔內(nèi)),、心內(nèi)注射給藥,。
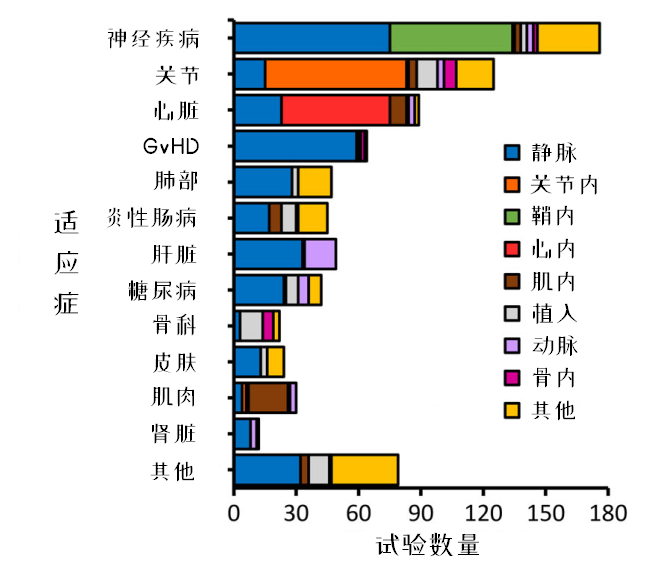 圖12:區(qū)分適應(yīng)癥來看給藥途徑的差異
圖12:區(qū)分適應(yīng)癥來看給藥途徑的差異
靜脈輸注的給藥方式使用頻率最高,但某些疾病有自己獨特的給藥方式,。比如關(guān)節(jié)的關(guān)節(jié)腔內(nèi)注射,,心臟的心肌注射,肌肉的肌內(nèi)注射,。值得注意的是,,在神經(jīng)疾病的給藥方式中,靜脈輸注的使用頻率依然超過了鞘內(nèi)輸注,,可能是出于安全考慮,。
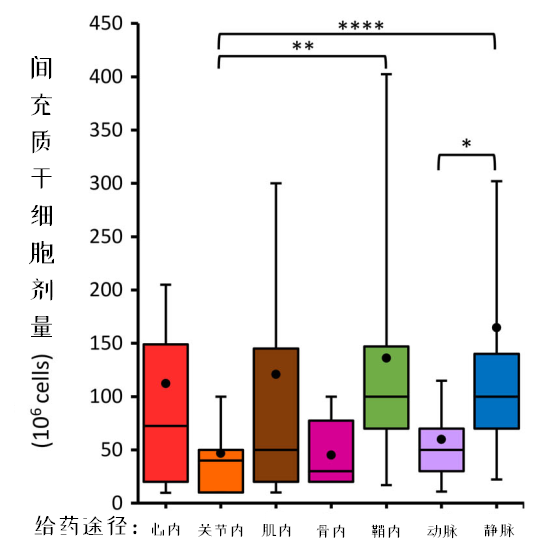
細胞劑量是影響臨床試驗療效的關(guān)鍵因素,,而在檢索的臨床試驗方案中,僅有53%的數(shù)據(jù)包含細胞劑量,。為了統(tǒng)一標準,,研究者將以每kg體重表示的細胞劑量,按人均70kg體重進行了換算,。
結(jié)果發(fā)現(xiàn),,靜脈輸注的細胞量最高,心臟內(nèi)和肌肉輸注的細胞量范圍跨度較大,,關(guān)節(jié)腔,、骨內(nèi)和動脈輸注的細胞量范圍跨度較小。 為了探索最佳劑量,,分析了同時出現(xiàn)有效劑量和無效劑量的研究,。結(jié)果,有16項靜脈輸注,、3項關(guān)節(jié)腔內(nèi)輸注的研究符合要求,。
同時發(fā)現(xiàn),劑量與效果之間的關(guān)系呈倒U型:過高和過低的劑量都效果不佳,。研究者推測免疫調(diào)節(jié)過度是過高劑量反而無效的原因,。
在16項采用靜脈輸注給藥的MSCs臨床試驗中,14項的最低有效劑量在70 - 190 X 10*6/人次之間,,超出這個區(qū)間的劑量無效,。 其余4項劑量遞增試驗結(jié)果表明,MSCs的最低有效劑量在一個更狹窄的區(qū)間內(nèi):100 - 150 X 10*6/人次之間,,劑量過低或過高都會降低其有效性,。
此外,3項關(guān)節(jié)腔給藥的臨床試驗結(jié)果顯示,,最低有效劑量范圍在50 - 100X10*6/人次之間,,10X10*6/人次和150X10*6/人次的劑量無效。
本次研究只歸納出,,靜脈輸注給藥和關(guān)節(jié)腔內(nèi)給藥這兩種給藥途徑可能適用的最低有效劑量區(qū)間,。
全球已開展了大量的MSCs臨床試驗,安全性得到廣泛驗證,,但上市的干細胞產(chǎn)品寥寥無幾,。
很多學者分析了這一現(xiàn)象,MSC治療機制尚不明確是一個原因,,更主要的是MSCs臨床試驗的個體化差異比較大,缺乏可比性,、可重復(fù)性差,。影響其治療效的因素太多:
?不同組織來源MSCs的異質(zhì)性
?不同的細胞制備工藝流程
?不同的傳代次數(shù)(這個用倍增時間更合適)
?不同的給藥途徑
?不同的劑量范圍
?不同的疾病差異
其中有些因素可以通過制定標準化來改善,。標準化產(chǎn)品,這涉及到細胞行業(yè)的痛點,。為了保護知識產(chǎn)權(quán),,很多公司都不會披露過多信息,使得比較不同研究變得很復(fù)雜,。
咨詢公司ZS Associates的CEO瑪麗亞·惠特曼(Maria Whitman)表示,,“在短期內(nèi),整個行業(yè)內(nèi)的標準化,,不太可能成為標準化的重點…”
劑量信息在臨床試驗數(shù)據(jù)中相對難獲取,,為什么難以獲取,或許我們可以做一個猜測,。劑量和給藥途徑,,在美國是受知識產(chǎn)權(quán)保護的,但在歐洲和中國是不被保護的,,這或許是原因,。
為此,小編咨詢了兩位科研人員,,但得到了矛盾的兩個結(jié)論(保護 vs 不保護),。于又咨詢了廣東華商律師事務(wù)所柏永權(quán)律師。柏律師表示,,根據(jù)《中華人民共和國專利法》第25條,,對于疾病的診斷和治療方法不授予專利權(quán)?!端幤饭芾矸▽嵤l例》第35條也有相關(guān)規(guī)定,,但保護范圍太窄,無法保護新用途藥物,,新劑量或新的給藥途徑,。
目前,MSCs臨床試驗的主要治療目標達成率低,。研究者建議,,在早期研究中就同時開展有效性的劑量研究,探索最低有效劑量,。
靜脈輸注后,,MSCs會在很短時間被免疫系統(tǒng)清除。研究者建議:以最低有效劑量間隔一段時間重復(fù)注射,,強化短期效應(yīng),,改善人體免疫微環(huán)境。
此外,研究者認為一些新技術(shù)會帶來積極的改變,。譬如封裝MSCs,,可以避免細胞間接觸,明確為旁分泌機制發(fā)揮作用,,且有利于慢性疾病治療,。
最后,研究者還給出了靜脈輸注的分組建議:
低劑量組 ~75X10*6/人次
中劑量組 ~150X10*6/人次
高劑量組 ~300X10*6/人次
參考內(nèi)容: Trends in mesenchymal stem cell clinical trials 2004‐2018: Is efficacy optimal in a narrow dose range? STEM CELLS Transl Med. 2019; 1– 11.